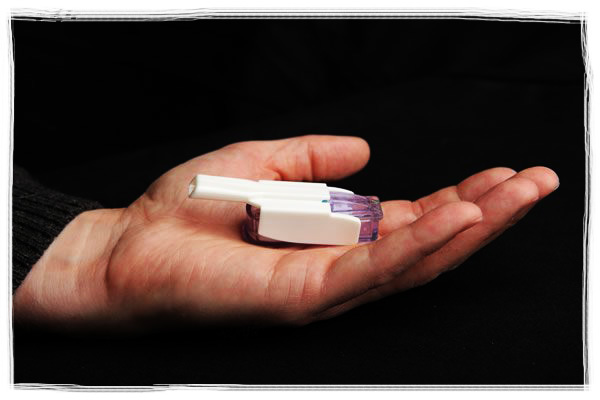
Uma nova fórmula de insulina por via inalatória foi aprovada pelo FDA (órgão dos EUA que controla alimentos e medicamentos) em Junho de 2014, chamada Affreza.
Afrezza é um medicamento que é inalado, e que chega à circulação através dos pulmões, e assim ajuda no controle da glicemia nos momentos das refeições. O FDA aprovou o tratamento do Diabetes tipo I e tipo II. É um subtipo de insulina em pó de ação ultra-rápida. O pico do nível de insulina na corrente sanguínea é em torno de 12 a 15 minutos após a administração. Nos pacientes com diabetes tipo I, é necessário a utilização associada da insulina de absorção lenta.
Na caixa do medicamento, há um alerta explicando que o Affreza pode causar constrição de vias aéreas em pacientes com DPOC ou Asma. Os pacientes com estas doenças não podem utilizar a medicação. Pacientes fumantes e aqueles que recentemente pararam de fumar (menos de 06 meses) também devem evitar o medicamento. Antes da utilização de Afrezza, é necessário um exame clínico detalhado e espirometria, para afastar potenciais doenças pulmonares em todos os pacientes.
As mais comuns reações adversas associadas ao medicamento (cerca de 2%) são hipoglicemia, tosse, irritação/dor de garganta.
Esta insulina inalável foi desenvolvida pela empresa MannKind, e ainda não foi lançado no Brasil, o que provavelmente deve ocorrer a partir do primeiro trimestre de 2015, e chegar no Brasil a partir de 2016.
Aproximadamente $1.8 bilhões foram gastos para o desenvolvimento desta medicação.
Antes da liberação desta medicação, foi comercializada entre 2005 e 2007, uma outra insulina inalável chamada Exubera, da empresa farmacêutica Pfizer. Entretanto, esta medicação foi retirada do mercado por falta de aceitação do público, provavelmente relacionado à falta de praticidade da medicação, que era do tamanho de uma lata de refrigerante e pelo elevado preço.
Infelizmente, ainda não se sabe se é uma medicação segura para pacientes com menos de 18 anos, portanto indicado somente para adultos.